Chương 3. Nhóm Cacbon - silic
Cacbon đioxit
- Chi tiết
- Chuyên mục: Chương 3. Nhóm Cacbon - silic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 15:39
- Viết bởi Nguyễn Văn Đàm
Cacbon đioxit có công thức phân tử là CO2. Nó còn có tên gọi khác là khí cacbonic hoặc anhiđrit cacbonic.
I. CẤU TẠO PHÂN TỬ VÀ TÍNH CHẤT VẬT LÍ
- Cấu tạo của CO2 là O=C=O.
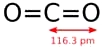
- Là khí không màu, vị hơi chua. Tan ít trong nước. CO2 khi bị làm lạnh đột ngột là thành phần chính của nước đá khô. Nước đá khô không nóng chảy mà thăng hoa nên được dùng để làm môi trường lạnh và khô, rất tiện lợi để bảo quản thực phẩm.
II. TÍNH CHẤT HOÁ HỌC
1. CO2 là oxit axit
- CO2 tan trong nước tạo thành axit cacbonic (là một điaxit rất yếu):
CO2 + H2O ↔ H2CO3
- CO2 tác dụng với oxit bazơ → muối:
CaO + CO2 → CaCO3 (t0)
- CO2 tác dụng với dung dịch bazơ → muối + (H2O)
NaOH + CO2 → NaHCO3
2NaOH + CO2 → Na2CO3 + H2O
Phản ứng của CO2 với dung dịch kiềm tạo thành muối nào tuỳ thuộc vào tỉ lệ số mol của 2 chất tham gia phản ứng. Bài toán về phản ứng với dung dịch kiềm cũng là dạng bài tập phổ biến nhất đối với CO2. Khi giải bài toán này, chúng ta thường dựa vào các định luật bảo toàn khối lượng, bảo toàn nguyên tố và bảo toàn điện tích.
2. CO2 bền, ở nhiệt độ cao bị nhiệt phân một phần và tác dụng được với các chất khử mạnh
2CO2 ↔ 2CO + O2 (t0)
CO2 + 2Mg → 2MgO + C
CO2 + C → 2CO
3. CO2 còn được dùng để sản xuất ure
CO2 + 2NH3 → NH4O - CO - NH2 (amoni cacbamat)
NH4O - CO - NH2 → H2O + (NH2)2CO (1800C; 200at)
III. ĐIỀU CHẾ
- Quá trình hô hấp của người và động vật:
C6H12O6 + 6O2 → 6CO2 + 6H2O
- Quá trình lên men bia rượu:
C6H12O6 → 2CO2 + 2C2H5OH
- Quá trình đốt cháy nhiên liệu:
CxHy + (x + y/4)O2 → xCO2 + y/2H2O
- Trong công nghiệp:
C + O2 → CO2 (đốt cháy hoàn toàn than cốc trong không khí)
CaCO3 → CaO + CO2 (10000C)
- Trong phòng thí nghiệm:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
IV. NHẬN BIẾT
Tạo kết tủa trắng với dung dịch nước vôi trong dư.
CO2 + Ca(OH)2 → CaCO3 + H2O
Mời các em tham khảo các bài tập sau cùng hochoaonline.net:
