Chương 9. Andehit, xeton, axit cacboxylic
Phản ứng đốt cháy axit cacboxylic
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Thứ bảy, 24 Tháng 1 2015 17:04
- Viết bởi Nguyễn Văn Đàm
Cũng giống như các chất hữu cơ khác, axit cacboxylic dễ dàng tham gia vào phản ứng đốt cháy:
- Phương trình phản ứng tổng quát:
CxHyOz + (x + y/4 - z/2)O2 → xCO2 + y/2H2O
- Dựa vào đặc điểm của phản ứng đốt cháy có thể kết luận được loại axit tham gia phản ứng.
Thường gặp nhất là các trường hợp sau:
Lí thuyết về axit cacboxylic
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:19
- Viết bởi Nguyễn Văn Đàm
I. ĐỊNH NGHĨA
- Các định nghĩa về axit cacboxylic:
+ Axit cacboxylic là hợp chất hữu cơ mà phân tử có nhóm - COOH liên kết với gốc hiđrocacbon, với H hoặc với nhau.
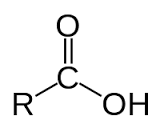
+ Axit cacboxylic là sản phẩm thu được khi thay nguyên tử H trong hiđrocacbon hoặc H2 bằng nhóm - COOH.
- Công thức tổng quát của axit:
Lý thuyết về anđehit - xeton
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:24
- Viết bởi Nguyễn Văn Đàm
A. ANĐEHIT
I. Định nghĩa
- Các định nghĩa có thể dùng với anđehit:
+ Anđehit là HCHC mà phân tử có nhóm - CHO liên kết với gốc hiđrocacbon, với H hoặc với nhau.
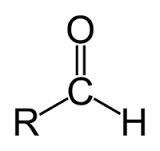
+ Anđehit là sản phẩm thu được khi thay nguyên tử H trong hiđrocacbon hoặc H2 bằng nhóm -CHO.
+ Andehit là HCHC mà phân tử có nhóm -CHO liên kết trực tiếp với C hoặc H
Phản ứng cộng hiđro của anđehit, xeton
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:26
- Viết bởi Nguyễn Văn Đàm
Do trong phân tử luôn có liên kết bội (ở nhóm chức cacbonyl) nên các anđehit và xeton đều có khả năng tham gia phản ứng cộng H2. Vì phản ứng của xeton có đặc điểm hoàn toàn tương tự với phản ứng cộng H2 của anđehit nên ở đây chỉ đề cập đến phản ứng cộng H2 vào anđehit.
R(CHO)x + xH2 → R(CH2OH)x (xúc tác Ni, t0)
Bài tập về phản ứng cộng H2 của anđehit, xeton thường gắn liền với bài tập ancol tác dụng với Na.
Chú ý:
Phản ứng của axit cacboxylic với các muối
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:28
- Viết bởi Nguyễn Văn Đàm
Các axit cacboxylic có khả năng phản ứng với các muối của axit yếu hơn (muối cacbonat, phenolat, ancolat) tạo thành sản phẩm là muối mới và axit mới. Hay gặp nhất là phản ứng của axit cacboxylic với các muối cacbonat và hiđrocacbonat.
Ví dụ:
R(COOH)x + xNaHCO3 → R(COONa)x + xH2O + xCO2
Khi giải các bài tập về phản ứng của axit cacboxylic với muối cacbonat hoặc hiđrocacbonat cần chú ý:
Phản ứng của axit cacboxylic với kiềm
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:31
- Viết bởi Nguyễn Văn Đàm
Trong phần tính axit của axit cacboxylic thì phản ứng của axit với kiềm là phản ứng hay gặp.
- Phương trình tổng quát của phản ứng:
R(COOH)x + xNaOH → R(COONa)x + xH2O
- Nếu axit tham gia phản ứng thuộc loại đơn chức:
RCOOH + NaOH → RCOONa + H2O
- Khi giải bài tập về phản ứng của axit cacboxylic với kiềm cần lưu ý:
Phản ứng este hóa axit cacboxylic
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:34
- Viết bởi Nguyễn Văn Đàm
Phản ứng este hóa với ancol là phản ứng quan trọng của axit cacboxylic.
- Phương trình phản ứng tổng quát:
R(COOH)x + R’(OH)t ↔ Ry(COO)xyR’x + xyH2O (xúc tác H2SO4, t0)
- Nếu axit cacboxylic và ancol tham gia phản ứng đều thuộc loại đơn chức (hay gặp) thì phản ứng có phương trình dạng:
RCOOH + R'OH ↔ RCOOH + H2O (xúc tác H2SO4, t0)
Phản ứng tráng bạc của anđehit
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:36
- Viết bởi Nguyễn Văn Đàm
Tráng bạc (còn gọi là phản ứng tráng gương) là một trong những phản ứng đặc trưng nhất của anđehit. Vì vậy bài tập về phản ứng tráng bạc cũng là dạng bài tập phổ biến và rất hay gặp khi làm về anđehit.
- Phương trình phản ứng tổng quát:
R(CHO)x + 2xAgNO3 + 3xNH3 + xH2O → R(COONH4)x + xNH4NO3 + 2xAg
→ Phản ứng chứng minh anđehit có tính khử và được dùng để nhận biết anđehit.
- Riêng HCHO có phản ứng:
HCHO + 4AgNO3 + 6NH3 + 2H2O → (NH4)2CO3 + 4NH4NO3 + 4Ag
Phản ứng của HCHO tạo ra các muối vô cơ chứ không phải muối của axit hữu cơ như các anđehit khác.
- Một số chú ý khi giải bài tập về phản ứng tráng bạc của anđehit:
Phản ứng đốt cháy anđehit
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:40
- Viết bởi Nguyễn Văn Đàm
Cũng giống như các hợp chất hữu cơ khác, anđehit dễ dàng tham gia vào phản ứng cháy khi được đốt nóng cùng oxi tạo ra sản phẩm cháy gồm CO2 và H2O:
CxHyOz + (x + y/4 - z/2)O2 → xCO2 + y/2H2O
Một số chú ý khi giải bài tập về phản ứng đốt cháy anđehit:
So sánh tính axit của axit hữu cơ
- Chi tiết
- Chuyên mục: Chương 9. Andehit, xeton, axit cacboxylic
- Được viết ngày Chủ nhật, 15 Tháng 3 2015 23:52
- Viết bởi Nguyễn Văn Đàm
1. Nguyên nhân axit cacboxylic có tính axit
Phân tử axit có nhóm cacbonyl C = O là nhóm hút e mạnh nên làm giảm mật độ e tự do trên nguyên tử O làm cho liên kết O - H bị phân cực hơn → dễ bị phân li thành H+ thể hiện tính axit.
RCOOH ↔ RCOO- + H+
(RCOOH + H2O ↔ RCOO- + H3O+)
2. So sánh tính axit của các axit hữu cơ
