Chương 5. Nhóm VIIA. Halogen
Lý thuyết về HCl
- Chi tiết
- Chuyên mục: Chương 5. Nhóm VIIA. Halogen
- Được viết ngày Thứ sáu, 27 Tháng 2 2015 22:15
- Viết bởi Nguyễn Văn Đàm
HCl và muối clorua là những hợp chất rất quan trọng của nguyên tố clo.
A. HIĐRO CLORUA, AXIT CLOHIĐRIC
1. Tính chất vật lí
- Hidro clorua là chất khí, không màu, mùi xốc tan nhiều trong nước tạo thành dung dịch axit mạnh HCl; Nặng hơn không khí.
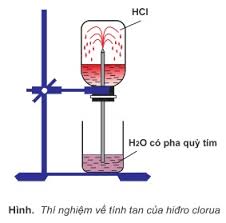
- Axit HCl là chất lỏng không màu, dễ bay hơi. Dung dịch axit HCl không màu, HCl đặc bốc khói trong không khí ẩm.
Axit HCl tác dụng với kim loại
- Chi tiết
- Chuyên mục: Chương 5. Nhóm VIIA. Halogen
- Được viết ngày Thứ sáu, 27 Tháng 2 2015 22:26
- Viết bởi Nguyễn Văn Đàm
Bài toán HCl với kim loại là bài toán phổ biến thường gặp. HCl tác dụng được với các kim loại đứng trước H2 trong dãy hoạt động hóa học của kim loại tạo ra sản phẩm là muối và H2 theo phương trình tổng quát:
2M + 2nHCl → 2MCln + nH2
Chú ý:
Hợp chất của halogen
- Chi tiết
- Chuyên mục: Chương 5. Nhóm VIIA. Halogen
- Được viết ngày Thứ sáu, 27 Tháng 2 2015 22:29
- Viết bởi Nguyễn Văn Đàm
I. HIĐRO HALOGENUA (HX) VÀ MUỐI HALOGENUA
1. Hiđro halogenua
- Tất cả đều là chất khí, tan nhiều trong nước, điện li hoàn toàn (trừ HF) tạo thành dung dịch axit mạnh.
- Thứ tự tính axit và tính khử tăng dần: HF < HCl < HBr < HI
- Tính axit mạnh của HCl, HBr và HI:
Clo
- Chi tiết
- Chuyên mục: Chương 5. Nhóm VIIA. Halogen
- Được viết ngày Thứ sáu, 27 Tháng 2 2015 22:31
- Viết bởi Nguyễn Văn Đàm
1. Tính chất vật lí

- Clo là chất khí, màu vàng lục, mùi xốc, nặng hơn không khí.
- Khí clo tan vừa phải trong nước tạo thành nước clo có màu vàng nhạt. Clo tan nhiều trong các dung môi hữu cơ.
- Khí clo độc.
Lý thuyết về halogen và hợp chất
- Chi tiết
- Chuyên mục: Chương 5. Nhóm VIIA. Halogen
- Được viết ngày Thứ sáu, 27 Tháng 2 2015 22:33
- Viết bởi Nguyễn Văn Đàm
I. ĐƠN CHẤT HALOGEN
1. Vị trí của nhóm halogen trong bảng tuần hoàn
- Nhóm halogen: nhóm VIIA.
- Nhóm halogen: gồm Flo (F), Clo (Cl), Brom (Br) và Iot (I).
2. Tính chất vật lí
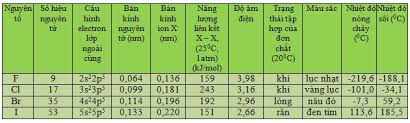
Phản ứng của HCl với hợp chất
- Chi tiết
- Chuyên mục: Chương 5. Nhóm VIIA. Halogen
- Được viết ngày Thứ sáu, 27 Tháng 2 2015 22:34
- Viết bởi Nguyễn Văn Đàm
Ngoài phản ứng với kim loại, tính axit của HCl còn được thể hiện khi cho HCl tác dụng với oxit bazơ, với bazơ và với các muối khác.
Cụ thể như sau:
1. Tác dụng với oxit kim loại → muối (trong đó kim loại giữ nguyên hóa trị) + H2O.
Fe3O4 + 8HCl → 4H2O + FeCl2 + 2FeCl3
Chú ý:
