Chuyên đề 17. Hợp chất hữu cơ chứa Nitơ
Lý thuyết về aminoaxit
- Chi tiết
- Chuyên mục: Chuyên đề 17. Hợp chất hữu cơ chứa Nitơ.
- Được viết ngày Thứ tư, 24 Tháng 12 2014 23:19
- Viết bởi Nguyễn Văn Đàm
I. ĐỊNH NGHĨA
- Aminoaxit là những hợp chất hữu cơ tạp chức trong phân tử có chứa đồng thời 2 nhóm chức: nhóm amino (NH2) và nhóm cacboxyl (COOH).
- Công thức tổng quát của aminoaxit: R(NH2)x(COOH)y hoặc CnH2n+2-2k-x-y(NH2)x(COOH)y.
Quan trọng nhất là các α - aminoaxit (các aminoaxit có các nhóm COOH và NH2 cùng gắn vào 1 nguyên tử C - C số 2). Hầu hết các aminoaxit thiên nhiên đều là các α - aminoaxit.
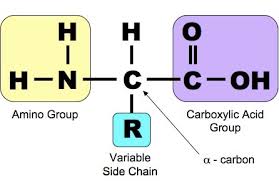
NH2-CH2-COOH Axit aminoaxetic (glixin hay glicocol)
CH3-CH(NH2)-COOH Axit aminopropionic (alanin)
HOOC-CH2-CH2-CH(NH2)-COOH Axit α-aminoglutaric (axit glutamic)
(CH3)2CHCH(NH2)COOH Axit α-aminoisovaleric (valin)
NH2(CH2)4CH(NH2)COOH Axit α,ε-điaminocaproic (Lysin)
HO-C6H4-CH2-CH(NH2)-COOH Axit α-amino-β(p-hidroxiphenyl)propanoic Tyrosin
II. TÍNH CHẤT VẬT LÍ
- Chất rắn, dạng tinh thể, không màu, vị hơi ngọt.
- Nhiệt độ nóng chảy cao, dễ tan trong nước vì amino axit tồn tại ở dạng ion lưỡng cực:
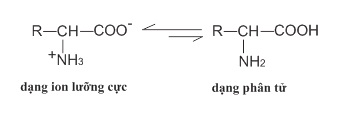
III. TÍNH CHẤT HOÁ HỌC
1. Sự phân li trong dung dịch
H2N-CH2-COOH ↔ H3N+-CH2-COO-
(ion lưỡng cực)
2. Aminoaxit có tính lưỡng tính
a. Tính axit
Tác dụng với bazơ mạnh tạo ra muối và nước:
NH2-CH2-COOH + KOH → NH2-CH2-COOK + H2O
Chú ý sử dụng phương pháp tăng giảm khối lượng khi giải bài tập.
b. Tính bazơ
Tác dụng với axit mạnh tạo muối.
NH2-CH2-COOH + HCl → ClNH3 - CH2 - COOH
Chú ý sử dụng phương pháp tăng giảm khối lượng và định luật bảo toàn khối lượng khi giải bài tập.
3. Phản ứng trùng ngưng của aminoaxit
nNH2-CH2-COOH → (- NH-CH2-CO-)n + nH2O (H+)
- Phản ứng trùng ngưng của 6-aminohexanoic (axit ε-aminocaproic) hoặc axit 7-aminoheptanoic (axit ω-aminoenantoic) với xác tác tạo thành polime thuộc loại poliamit.
- Từ n aminoaxit khác nhau có thể tạo thành n! polipeptit chứa n gốc aminoaxit khác nhau; nn polipeptit chứa n gốc aminoaxit.
4. Phản ứng với HNO2
HOOC-R-NH2 + HNO2 → HOOC-R-OH + N2 + H2O
5. Phản ứng este hoá
NH2-CH2-COOH + ROH → NH2-CH2-COOR + H2O (khí HCl)
Chú ý
- Aminoaxit có làm đổi màu quỳ tím hay không tùy thuộc vào quan hệ giữa số nhóm COOH và số nhóm NH2 có trong phân tử aminoaxit:
+ Nếu phân tử aminoaxit có số nhóm COOH = số nhóm NH2 → aminoaxit không làm đổi màu quỳ tím.
+ Nếu phân tử aminoaxit có số nhóm COOH > số nhóm NH2 → aminoaxit làm đổi màu quỳ tím thành đỏ.
+ Nếu phân tử aminoaxit có số nhóm COOH < số nhóm NH2 → aminoaxit làm đổi màu quỳ tím thành xanh.
- Các phản ứng do muối của aminoaxit tác dụng với dung dịch axit hoặc dung dịch kiềm.
NH2-CH2-COOK + 2HCl → NH3Cl-CH2-COOH + KCl
NH3Cl-CH2-COOH + 2KOH → NH2-CH2-COOK + KCl + H2O
IV. ĐIỀU CHẾ
Thủy phân protit
(-NH-CH2-CO-)n + nH2O → nNH2-CH2-COOH
Mời các bạn tham khảo một số bài tập sau cùng hochoaonline.net:




