Chuyên đề 3. Phi kim 1 - Nhóm VIIA và VIA
Lưu huỳnh đioxit
- Chi tiết
- Chuyên mục: Chuyên đề 3. Phi kim 1- Nhóm VIIA và VIA
- Được viết ngày Thứ bảy, 07 Tháng 2 2015 14:21
- Viết bởi Nguyễn Văn Đàm
Lưu huỳnh đioxit (SO2) còn có thể được gọi là (sunfu đioxit, khí sunfurơ, lưu huỳnh (IV) oxit, sufu (IV) oxit, anhiđrit sunfurơ).
1. Tính chất vật lí
Là chất khí không màu, nặng hơn không khí, mùi hắc, độc, tan và tác dụng được với nước.
2. Tính chất hóa học
a. SO2 là oxit axit
- Tác dụng với nước:
SO2 + H2O ↔ H2SO3
- Tác dụng với dung dịch bazơ (có thể tạo thành 2 loại muối sunfit và hiđrosunfit):
SO2 + NaOH → NaHSO3
SO2 + 2NaOH → Na2SO3 + H2O
Để xác định muối nào được tạo ra trong quá trình phản ứng phải tính tỉ lệ số mol của 2 chất tham gia phản ứng.
- Tác dụng với oxit bazơ → muối:
SO2 + CaO → CaSO3 (t0)
b. SO2 vừa là chất khử, vừa là chất oxi hóa
SO2 vừa có tính khử, vừa có tính oxi hoá vì S trong SO2 có mức oxi hóa trung gian +4.
* SO2 là chất oxi hóa:
SO2 + 2H2S → 3S + 2H2O
* SO2 là chất khử:
2SO2 + O2 ↔ 2SO3 (V2O5, 4500C)
Cl2 + SO2 + 2H2O → H2SO4 + 2HCl
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
3. Điều chế
- Đốt cháy lưu huỳnh:
S + O2 → SO2 (t0)
- Đốt cháy H2S trong oxi dư:
2H2S + 3O2 → 2H2O + 2SO2
- Cho kim loại tác dụng với H2SO4 đặc nóng:
Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
- Đốt quặng:
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
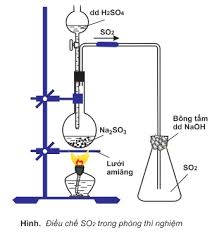
- Trong phòng thí nghiệm dùng phản ứng của Na2SO3 với dung dịch H2SO4:
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
4. Nhận biết
- Làm quỳ tím ẩm chuyển thành màu đỏ.
- Làm mất màu dung dịch nước brom, dung dịch thuốc tím…
SO2 + 2H2O + Br2 → 2HBr + H2SO4
5. Ứng dụng
- Sản xuất axit sunfuric.
- Tẩy trắng giấy, bột giấy.
- Chống nấm mốc cho lương thực, thực phẩm.
Ngoài các ứng dụng trên, SO2 còn là chất gây ô nhiễm môi trường. Nó là nguyên nhân gây ra hiện tượng mưa axit.
Hochoaonline.net giới thiệu đến bạn đọc các bài tập về SO2: