Chuyên đề 3. Phi kim 1 - Nhóm VIIA và VIA
Axit sunfuric loãng
- Chi tiết
- Chuyên mục: Chuyên đề 3. Phi kim 1- Nhóm VIIA và VIA
- Được viết ngày Thứ bảy, 07 Tháng 2 2015 14:40
- Viết bởi Nguyễn Văn Đàm
Axit sunfuric là một trong những axit vô cơ quan trọng hàng đầu trong đời sống và sản xuất.
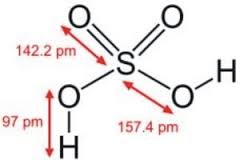
1. Tính chất vật lí
- H2SO4 là chất lỏng, nhớt, nặng hơn nước, khó bay hơi và tan vô hạn trong nước.
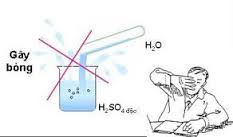
- H2SO4 đặc hút nước mạnh và tỏa nhiều nhiệt nên khi pha loãng phải cho từ từ axit đặc vào nước mà không làm ngược lại vì có thể gây bỏng. H2SO4 có khả năng làm than hóa các hợp chất hữu cơ.
2. Tính chất hóa học
H2SO4 loãng là một axit mạnh, có đầy đủ các tính chất hóa học chung của axit:
- Làm quỳ tím chuyển thành màu đỏ.
- Tác dụng với kim loại đứng trước H (trừ Pb) → muối sunfat (trong đó kim loại có hóa trị thấp) + H2:
Fe + H2SO4 → FeSO4 + H2
Chú ý:
nH2 = nH2SO4
mmuối = mkim loại + mH2SO4 - mH2 = mkim loại + 96nH2
- Tác dụng với oxit bazơ → muối (trong đó kim loại giữ nguyên hóa trị) + H2O
FeO + H2SO4 → FeSO4 + H2O
Chú ý:
nH2SO4 = nH2O = nO (trong oxit)
mmuối = moxit + mH2SO4 - mH2O = moxit + 98nH2SO4 - 18nH2O
= moxit + 80nH2SO4 = moxit + 80n(O trong oxit)
- Tác dụng với bazơ → muối + H2O
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
(phản ứng của H2SO4 với Ba(OH)2 hoặc bazơ kết tủa chỉ tạo thành muối sunfat).
Cu(OH)2 + H2SO4 → CuSO4 + 2H2O
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
- Tác dụng với muối → muối mới (trong đó kim loại giữ nguyên hóa trị) + axit mới
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
Chú ý: Thường dùng phương pháp tăng giảm khối lượng khi giải bài tập về phản ứng của axit sunfuric với muối.
3. Điều chế
FeS2 hoặc S → SO2 → SO3 → H2SO4
4. Nhận biết
- Làm đỏ giấy quỳ tím.
- Tạo kết tủa trắng với dung dịch Ba2+
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
(các muối sunfat đều dễ tan trừ BaSO4, PbSO4 và SrSO4 không tan; CaSO4 và Ag2SO4 ít tan).
5. Ứng dụng
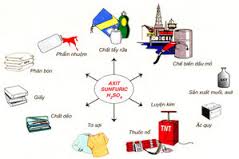
Axit sunfuric là hóa chất hàng đầu trong nhiều ngành sản xuất: phẩm nhuộm, sơn, luyện kim, phân bón, chất dẻo, chất tẩy rửa...
Hochoaonline.net giới thiệu đến bạn đọc các bài tập tham khảo sau đây: